
Em 1987, com a descoberta por Ignarro, Moncada e outros pesquisadores de que o óxido nítrico (NO) era o gás vasodilatador derivado das paredes internas dos vasos (endotélio), responsável direto pelo controle da pressão sanguínea, esta pequena molécula, diatômica, escapou das mãos e mentes dos químicos de coordenação, químicos da atmosfera e engenheiros químicos e, veloz e vigorosamente, inundou, abalou e alicerçou as bases da Medicina moderna(figura 1). Nos cinco anos seguintes, o Web of Sciences (Institute for Scientific Information) registrou a publicação de mais de seis mil artigos sobre o NO, dezessete mil no qüinqüênio seguinte e mais de vinte mil nos últimos cinco anos. Em 1992, a American Association for the Advancement of Science elegeu o NO como a molécula do ano (Science, 1992) e Ignarro com outros dois cientistas ganharam o Nobel de Medicina de 1998.
O NO já era conhecido por Faraday e Gay Lussac, no século XIX, como um gás facilmente difusível no ar e líquidos, paramagnético (portanto um radical livre), cerca de dez vezes mais solúvel em solventes orgânicos que em água, tal como o oxigênio molecular (O2). Sua alta reatividade química com compostos tiólicos (R-SH), levando à formação de S-nitrosotióis (R-SNO), e rápida coordenação a metais de transição tais como íons de ferro e cobre, associadas ao antigo uso de medicamentos nitrados (R-NO2) e nitrosados (R-NO), do tipo de nitroprussiato de sódio, nitrito de amila e mesmo a nitroglicerina como anti-hipertensivos, foram pistas importantes para a descoberta da natureza química do endothelium derived relaxing factor (fator EDRF), identificado como sendo o NO. O achado de Ignarro e Moncada foi o ponta-pé inicial para a revelação de rico e sofisticado repertório de funções biológicas do NO, algumas benéficas e outras deletérias.O NO regula o tônus e a permeabilidade vascular, a adesão celular, a neurotransmissão, a adesão plaquetária, a broncodilatação, o sistema imunológico e a função renal, mas inibe a atividade de várias metaloenzimas, induz a peroxidação das membranas das células e lesão química do DNA, depleta os estoques de antioxidantes e aumenta a suscetibilidade de tecidos à radiação, metais pesados e agentes alquilantes. Portanto, tal como o oxigênio molecular, o NO comporta-se como uma faca de dois gumes: provê vida, mas também mata.
O aminoácido arginina e íons nitrito são as fontes celulares de NO. Enzimas denominadas óxido nítrico sintases (NOS), presentes em quase todos os tipos de células (neuronais, epiteliais, macrófagos, etc), catalisam a oxidação de argina por O2 levando à produção de NO. Por outro lado, o suco gástrico e tecidos isquêmicos (como músculo cardíaco) ou inflamados por bactérias, têm pH muito baixo (< 4) e, nestas condições, o nitrito presente se protona ao ácido nitroso, que sofre dismutação a ácido nítrico e NO. Dentro e fora das células, NO e O2 travam intenso e complexo diálogo químico através de seus produtos de reação - NO2, O2 (ânion radical superóxido), HO (radical hidroxila), ONOO- (ânion peróxinitrito), CO3 (ânion radical carbonato) - através de inúmeras reações de oxidação, nitração e nitrosação, que desencadeiam respostas biológicas de vida e morte. Para ilustrar a altíssima capacidade oxidante destas espécies de oxigênio e nitrogênio, basta mencionar que o radical hidroxila (Eº = +2,3 V), o radical carbonato (Eº = +1,8 V) e o peróxinitrito (Eº = +1,4 V) têm potenciais de redução comparáveis ao do íon permanganato (Eº = + 1,5 V), dicromato (Eº = +1,3 V) e Ce4+ (Eº = + 1,6 V); lembro que quanto mais positivo é o potencial padrão de redução (Eº ), mais fortemente oxidante é a espécie. Como ambos os gases, O2 e NO, são mais solúveis em ambientes apolares, hidrofóbicos, é de se esperar que sua química oxidativa e nitrosativa ocorra preferencialmente em tecidos ou estruturas mais gordurosos como é o caso do cérebro, membranas celulares e ateromas.
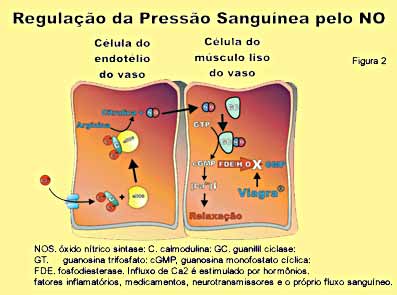
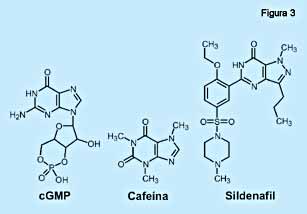
A (bio)química anunciada e aplicada do NO colocou vários medicamentos nas prateleiras das farmácias. Sem sombra de dúvidas, o de maior impacto foi um análogo de cafeína chamado sildenafil (Viagra®, do laboratório Pfizer)- um vasodilatador peniano amplamente utilizado hoje no tratamento da impotência masculina, o qual trouxe felicidade e equilíbrio para milhões de famílias. O mecanismo da vasodilatação inicia-se pela ativação da NO sintase por vários sinais da corrente sanguínea e o seu produto, o NO, se difunde para a camada muscular subjacente ao endotélio onde se liga ao íon de ferro da guanilato sintase, ativando-a (figura 2). Esta enzima produz o cGMP (guanosina monofosfato cíclico), uma molécula mensageira da captação de cálcio por estruturas subcelulares, impedindo a contração muscular que sabidamente é dependente de cálcio. O músculo do corpo cavernoso então relaxa, permitindo maior afluxo do sangue e o conseqüente enrijecimento do pênis. Acontece que a vida média do cGMP é diminuída pela ação hidrolítica de uma fosfodiesterase que o transforma em GMP, não ativo na contração muscular, e moléculas parentes da cafeína, como é o caso do sildenafil, inibem esta enzima (figura 3). O resultado final é o aumento da vida média do cGMP e, conseqüentemente, aumento do vigor e tempo de endurecimento do pênis. Recentemente, mais dois inibidores da fosfodiesterase do cGMP, análogos do sildenafil, foram lançados no mercado para tratamento da impotência masculina: o Tadalafil (Cialis®, do laboratório Eli Lilly) e o Vardenafil (Levitra®, dos laboratórios Bayer e GlacoSmith-Kline).
Centenas de grupos de pesquisa em todo o mundo continuam a pesquisa de novas fontes químicas e enzimáticas de espécies reativas de oxigênio e nitrogênio, estudam sua reatividade com biomoléculas e estruturas celulares e buscam aplicações deste conhecimento para intervir de forma inteligente e eficaz na saúde humana. No Brasil, destacaria a atuação de vários químicos que têm dado relevantes contribuições à química e aplicações médicas do óxido nítrico e seus derivados oxidantes. No Instituto de Química da USP, a Profª. Ohara Augusto, química especialista na técnica de Ressonância Paramagnética de Elétron (EPR), provou a formação de radical hidroxila na homólise do ácido peróxinitroso, evidenciou a formação do radical carbonato em misturas peróxinitrito/carbonato, detectou radicais de enxofre em várias proteínas e, recentemente, elucidou eventos radicalares importantes na leismaniose. Foi conferencista convidada da reunião da American Chemical Society de 2002. No HEMOCENTRO (São Paulo), os trabalhos do químico Dr. Hugo Pequeno Monteiro sobre várias rotas de sinalização química celular química, envolvendo enzimas-chave do metabolismo humano, deram-lhe também projeção internacional. O Drº Marcelo Ganzarolli de Oliveira, no IQ da UNICAMP, está sintetizando novos doadores de NO e imobilizando-os nos stents usados em angioplastia para prevenir processo inflamatório precursor de re-estenose, em colaboração com o Drº Francisco Laurindo, do INCOR. Este último pesquisador tem se destacado nas reuniões da American Heart Association, como descobridor de processos radicalares envolvidos na lesão mecânica produzida pelo cateter na angioplastia. Na Faculdade de Ciências Farmacêuticas da USP, a Drª Dulcinéia Abdalla elucidou mecanismos importantes implicados na oxidação do LDL e conseqüente formação de ateromas (placas) nos vasos e, no nosso Instituto, meu grupo de pesquisa tem estudado reações de metabólitos carbonílicos e imínicos, acumulados nos tecidos de pacientes portadores de várias patologias (exemplo: porfiria aguda intermitente, diabetes, cetoacidoses), com espécies reativas de oxigênio e nitrogênio, em especial o peróxinitrito. Estes são apenas alguns exemplos de pesquisas realizadas no Brasil nesta área do conhecimento, ainda em crescimento exponencial, segundo o banco de dados do National Institute of Health (USA) e extremamente promissora.
Etelvino Bechara é Professor Titular do Instituto de Química da USP e venceu o Prêmio Fritz Feigl deste ano. Contatos podem ser feitos pelo fax (011) 3815-5579 ou pelo e-mail: ebechara@quim.iq.usp.br